资讯中心
作者:香雪生命科学-石丹枫
发布时间:2021-10-27
阅读:15295
你听说过免疫检查点(Immune checkpoint)吗?
我们知道,外界病毒、细菌等异物入侵,或体内细胞衰老、死亡、病变都会激活人体的免疫系统。免疫系统活化后开始清除“异己分子”。而免疫系统如果过度活化,就会伤害正常细胞,引起自身免疫病。所谓一物降一物,免疫检查点就是免疫系统中的抑制性通路,由配体/受体的相互作用所调控。它对于维持自身免疫耐受、调节生理性免疫应答的持续时间和幅度起重要作用。免疫检查点分子的概念也在很早就被提出,它的重要功能之一就是控制免疫系统不要“滥杀无辜”。
免疫检查点分子有多个,今天介绍其中的一个:CTLA-4(Cytotoxic T- Lymphocyte Antigen 4),全名为细胞毒性T淋巴细胞相关抗原4,又名CD152,是由CTLA-4基因编码的表达于活化的T细胞表面的一种跨膜蛋白。
关于CTLA-4的研究,可以追溯到很久以前,且有一个名字不得不被提起,他就是美国著名免疫学家詹姆斯·艾利森(James P Allison)。早在1995年,加拿大华裔科学家Tak Mak和美国Arlene Sharpe的团队分别报道了CTLA-4基因敲除小鼠会出现严重的自身免疫病并迅速死亡的现象[1,2]。当人们将CTLA-4关注点放在自身免疫病领域时,詹姆斯·艾利森教授却独具慧眼地发现了CTLA-4在肿瘤免疫应答系统中的价值。1996年,他率领团队在小鼠实验中证明,用CTLA-4抗体可增强免疫并治疗动物肿瘤[3]。当团队里的其他人还在继续小鼠实验及探索抗肿瘤活性背后的分子机制时,艾利森教授已经在思考其他的事情:他迫切地想要实现抗CTLA-4活性单抗的临床试验。为了说服公司研发人源化的抗CTLA-4活性单抗并进行肿瘤临床试验,艾利森教授进行了各种“花言巧语”般的游说,最终,找到了在Medarex公司工作的好友Alan Korman,与自己一同开发人源化的抗CTLA-4活性单抗。Medarex全权负责了人源化的抗CTLA-4活性单抗的开发,然后进行一期临床试验,以及之后的试验。这一切,正在改变历史。后来的事我们都知道了,伊匹单抗诞生了。詹姆斯·艾利森教授也因此于2018年获得了诺贝尔生理学或医学奖。

图1. 2018年诺贝尔生理学或医学奖授予两位免疫学家:美国的詹姆斯·艾利森(James P Allison)与日本的庶佑(Tasuku Honjo),以表彰他们“发现负性免疫调节治疗癌症的疗法方面的贡献”。这一发现为癌症治疗开创了全新的免疫治疗思路——释放免疫系统自身的能力来攻击肿瘤。(来源:The official website of the Nobel Prize)
CTLA-4是负性免疫调节通路中的一个关键分子,我们可以称之为免疫系统的“分子刹车”。癌症为了躲避免疫系统的监控,会利用免疫系统的“分子刹车”来抑制机体对恶性肿瘤细胞的免疫应答。詹姆斯·艾利森认为,如果可以暂时抑制分子刹车CTLA-4的活性,就能提高免疫系统对肿瘤细胞的攻击性,达到负负得正的效果。这不同于传统的免疫疗法思路致力于刺激机体的免疫系统,强化其对癌症的免疫应答。如果把传统的免疫疗法思路比喻成“踩油门”,那么免疫检查点抑制剂疗法就是“释放刹车”。这是一个全新的思路。
为了帮助大家更好地理解这一原理,我们需要先了解正常情况下,T细胞是如何被激活的。
T细胞的活化需要两条信号通路的共同激活:①T淋巴细胞受体(TCR)与抗原呈递细胞(APC)呈递的MHC-抗原肽复合物相结合;②抗原呈递细胞(APC)的B7分子配体(B7-1或B7-2)与T细胞表面的共刺激分子CD28相结合。
CTLA-4高表达于调节性T淋巴细胞(Treg)和激活的T淋巴细胞上,与T细胞表面的共刺激分子CD28具有高度同源性,两者共用抗原呈递细胞(APC)的B7分子配体,且CTLA-4与B7的亲和力更强。当机体免疫系统被激活后,CTLA-4通过复杂的机制被上调,过量表达的CTLA-4与自己的“亲兄弟”CD28竞争性结合B7分子配体,抑制共刺激信号,诱导T细胞无反应性,以及介导Treg的抑制功能,从而抑制了机体的免疫反应。CTLA-4在多种肿瘤浸润的T细胞中过表达,导致肿瘤生长失控。而靶向CTLA-4的抑制剂可阻断CTLA-4与B7结合,阻止T细胞抑制信号产生,从而增强特异性抗肿瘤的免疫反应。
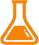
图2. CTLA-4免疫负性调节的原理与CTLA-4抗体的应用原理(来源:生物制药小编)
当T细胞被激活后,CTLA-4的表达上调,并与共刺激分子CD28竞争性结合B7配体,抑制了共刺激信号,从而抑制了机体的免疫反应(图中用Inhibitory表示);如果用CTLA-4的抗体进行封闭,可阻止抑制信号的产生,释放T细胞的活性,从而增强免疫反应(图中用Stimulatory表示)。
2011年首个CTLA-4单抗Ipilimumab(伊匹单抗)获FDA批准用于治疗晚期黑色素瘤,成为第一个用于肿瘤治疗的免疫检查点药物,开启了肿瘤免疫检查点抑制剂新时代。与明星靶点PD-1/PD-L1药物上市后“百花齐放”不同,CTLA-4抑制剂研究起步稍早,但目前此类药物却仍然只有Ipilimumab获批上市,足见除了Ipilimumab外全球范围内其他CTLA-4抑制剂研究进度较慢,绝大多数研究仍处于临床探索阶段。遇到的主要问题也跟PD-1抗体药类似,那就是应答率有限。未来可以做的是提高免疫检查点阻断的效率以及免疫检查点抑制剂组合疗法来使那些单独阻断剂不能治疗的病人获得持久的抗肿瘤响应。
参考文献:
[1]Tivol, E. A., Borriello, F., Schweitzer, A. N., Lynch, W. P., Bluestone, J. A., & Sharpe, A. H. (1995). Loss of CTLA4 leads to massive lymphoproliferation and fatal multiorgan tissue destruction, revealing a critical negative regulatory role of CTLA-4. Immunity, 3(5), 541-547.
[2] Waterhouse P, Penninger JM, Timms E, Wakeham A, Shahinian A, Lee KP, Thompson CB, Griesser H, Mak TW. Lymphoproliferative disorders with early lethality in mice deficient in Ctla-4.[J]. Science, 1995, 270(5238):985-985.
[3] Arthur A Hurwitz , Timothy J. Sullivan , Matthew F Krummel , Raymond A Sobel , James P Allison. Specific blockade of CTLA-4/B7 interactions results in exacerbated clinical and histologic disease in an actively-induced model of experimental allergic encephalomyelitis[J]. Journal of Neuroimmunology, 1997, 73(1-2):57-62.