资讯中心
作者:香雪精准医疗--马瑞娟
发布时间:2020-11-30
阅读:15490
癌症是夺走人们生命的罪魁祸首之一,许多人谈癌色变的,人类与癌症的斗争也从未停止过。据全球医官网权威报道:全球癌症年报显示,2020年全球预计新发癌症病例1890万例,死亡病例968万例。癌症防治已成为重要公共卫生问题,免疫治疗是目前公认的除了手术、化疗和放疗之外能治疗肿瘤的有效方法之一,过激性免疫治疗已成为国内外研究的热点问题。
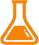
目前,过继性免疫细胞治疗应用的比较多的免疫细胞有T淋巴细胞、NK细胞和DC细胞,T淋巴细胞被认为是机体唯一能特异性识别杀伤肿瘤细胞的免疫细胞。人的 T 淋巴细胞根据其细胞表面受体 (TCR) 结构的不同,可以分为 αβ (如CD4、CD8等)和γδ T细胞两大类。人外周血淋巴细胞以αβ T细胞为主,γδ T细胞一般只占1%~5%。由于细胞表面受体结构的差异,这两类细胞的功能以及在免疫应答中的响应机制也有显著差异,比如αβ T 细胞对抗原的识别依赖于MHC分子,而γδ T细胞对抗原的识别则不需要MHC分子的参与,且其本身就具有抗原提呈特性与功能。
目前最火热的细胞疗法,当属TCR T、CAR T,这个T指的是αβ T细胞,然而有关注到γδT细胞在免疫调节、肿瘤免疫监视和特异性初次免疫应答中所起的作用已不断被认识,应用 γδT 细胞进行肿瘤细胞免疫治疗的研究也有许多报道,我们一起来看看吧。
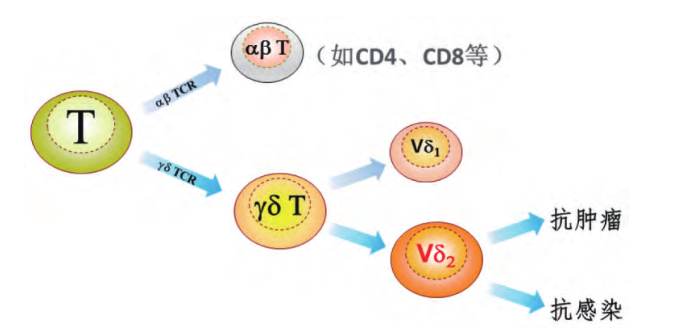
γδT细胞受体TCR γδ是由γ链和δ链组成的异二聚体,γ链和δ链分别由 γ基因和δ基因编码。每条肽链都有2个免疫球蛋白样结构域 :氨基末端可变区(V 区)结构域和 1 个羧基末端稳恒定区(C区)结构域。γ链含有10个V基因片段、2个D基因片段和2个J基因片段,δ链含有7个V基因片段和2 个J基因片段,VJD/VJ 基因片段重排后表达多种γ链和δ链。但由于γδ T细胞亚群往往只使用特定的VγVδ和连接区(J区)序列的组合,便导致了TCR γδ 多样性不及TCR αβ。但TCR γδ实力也不容小觑,γδ T细胞可以通过其细胞表面的NK细胞受体,ADCC效应及其分泌的细胞因子(IFN-γ,TNF-α)等方式直接杀伤肿瘤细胞(Fig.1)除了直接杀伤肿瘤细胞,γδ T细胞还可以通过各种力所能及的方式激活B/DC/αβ T/NK细胞(如:充当抗原提呈细胞激活αβ T 细胞,或由4-1BB共刺激途径诱导NK 介导的抗肿瘤细胞毒性等),进而实现对肿瘤的间接杀伤。
Fig 1. Antitumour γδ T cell functions and their regulation
自体 γδ T 细胞在抗肿瘤免疫治疗中的安全性和有效性在大量的临床试验中已经得到确认,对于不同类型的癌症均表现出较好的治疗效果,如白血病/淋巴瘤、黑色素瘤、肾细胞癌、前列腺癌、乳腺癌、非小细胞肺癌、结直肠癌、多发性骨髓瘤、胃肠道肿瘤、卵巢癌、宫颈癌、骨癌等。
一项应用治疗 6 位接受过肺转移瘤切除术的结直肠癌患者临床试验,将患者自体 γδT 细胞体外用IL-2 和唑来磷酸扩增后,每周一次回输给患者,总共回输8次。治疗后 5 例患者达到部分缓解,1 例患者为稳定。Bennouna等对10例肾细胞癌患者应用 γδ T 细胞进行过继性免疫治疗后,6例患者病情保持稳定,且与对照组相比肿瘤体积明显缩小,毒副反应轻微,生存期也有所延长,治疗效果显著。Kobayashi等应用自体γδT细胞治疗7例晚期肾癌,每周或每2周回输一次,共6~12次;利用肿瘤倍增时间 (doubling time, DT)、电子计算机断层扫描并结合流式分析结果观察疗效,结果显示5例患者的DT延长,3例患者外周血中γδT细胞数量增加,对外来抗原应答加强,而没有明显毒副作用。此外,11例晚期肾细胞癌患者接受自体γδ T细胞治疗后,3~5d外周血中γδ T细胞数量就达到峰值,肿瘤倍增时间延长,肿瘤体积明显缩小,最终1例完全缓解、5例稳定、5例进展期。
目前已有不少利用自体 γδ T 细胞进行抗肿瘤治疗的临床研究,但是关于同种异体 γδ T 细胞的治疗应用才刚刚在国际上兴起。相比患者自体免疫细胞,来自健康人的同种异体免疫细胞具有更大的优势。而且 γδ T 细胞由于其对癌细胞的识别不需 MHC 分子的参与,可以直接选择性识别、杀伤癌细胞,更重要的是,不同人来源的 γδ T 细胞没有排异性。有研究团队团队近期的临床研究验证了同种异体 γδ T 细胞的这些特性。来自健康人的 PBMC 体外扩增后过继给肿瘤患者,安全、无排斥、无细胞因子风暴。
γδT细胞能显著抑制肿瘤细胞的生长,同时对病毒 ( 如乙肝病毒 )、细菌 ( 如结核菌 ) 感染具有治疗作用,随着γδT 细胞的亚类不断被发现,为γδT细胞的研究提供了广阔的前景。另外,也说明在特定疾病中,可能还存在着发挥特定功能的γδ T细胞,还需要今后更多、更深入的研究去探索,以便为各种疾病的治疗,提供更多可供选择的方案。
1. Nat Rev Cancer. 2019 Jul;19(7):392-404. doi: 10.1038/s41568-019-0153-5
2.Suzuki A, Hanada T,Mit suyama K et al .CIS3/SOCS3/SSI3 plays a neg-ative regulatory role inSTAT3 activation and intestional inflammation[ J] .ExpMed, 2001;193( 4) :471-481.
3.Meissner H C,Leung D M .Superantigens, comentional antigens and the e-tiology of Kawasaki syndrome[ J] .Pediatr Infect Dis J, 2000;19( 2) :91-94.
4.Yu H, Jove R.The STATs of cancer-new molecular targets come of age[ J] .Nat Rev Cancer, 2004;4( 2) :97-105.
5.Schindler C W.Series introduction, JAK-STAT signaling in human disease[ J] .Clin Invest, 2002;109( 9) :1133-1137.
6.Murray P J.The JAK-STAT3 signaling pathway :input and output integra-tion[ J] .Immunol, 2007;178 (5) :2623-2629.
7.Klover P J, Zimmers T A, Koniaris L G et al .Chronic exposure to inter-leukin-6 causes hepatic insulin resistance inmice[ J] .Diabetes,2003;52 ( 11) :2784-2789.
8.Legut M, Cole DK, Sewell AK. The promise of gamma delta T cells and the gamma delta T cell receptor for cancer immunotherapy[J]. CellMol Immunol, 2015, 12(6):656-668.
9.Dieli F, Vermijlen D, Fulfaro F, et al. Targeting human {γ}δ} T cells with zoledronate and interleukin-2 forimmunotherapy of hormone-refractory prostate cancer.Cancer Res, 2007, 67: 7450-7
10.Bennouna J, Bompas E, Neidhardt EM, et al. Phase-I study of Innacell γδ, an autologous cell-therapy product highly enriched in γ9δ2 T lymphocytes, in combination with IL-2, in patients with metastatic renal cell carcinoma.Cancer Immunol Immunother, 2008, 57: 1599-609
11.Kobayashi H, Tanaka Y, Yagi J, et al. Safety profile and anti-tumor effects of adoptive immunotherapy using γ-δ T cells against advanced renal cell carcinoma: a pilot study.Cancer Immunol Immunother, 2007, 56: 469-76
12.Kobayashi H, Tanaka Y, Yagi J, et al. Phase I/II study of adoptive transfer of γδ T cells in combination with zoledronic acid and IL-2 to patients with advanced renal cell carcinoma. Cancer Immunol Immunother, 2011, 60:1075-84