资讯中心
作者:香雪生命科学研究中心-王宜
发布时间:2019-08-27
阅读:14828
软组织肉瘤 ( soft tissues arcomas, STS ) 是一类起源于结缔组织 ( 除骨与软骨 ) 的恶性肿瘤,包括皮下组织、肌肉、肌腱、血管、结缔组织间隙以及空腔器官支柱基质等。发病率大约( 1.28~1.72 ) / 10 万, 约占成人恶性肿瘤的 1% ,占儿童恶性肿瘤的15%。 软组织肉瘤的细胞起源为原始间叶干细胞,位于非阶段性中胚层,故可以生长在身体不同部位。按身体不同部位的发病几率排列为下肢、躯干、头颈、上肢,后腹膜也可出现脂肪肉瘤和纤维肉瘤。
世界卫生组织WHO将软组织肉瘤分为 50多种亚型。常见的亚型有恶性纤维组织细胞瘤、胃肠间质瘤、脂肪肉瘤、平滑肌肉瘤、滑膜肉瘤和恶性外周神经鞘瘤等,其中横纹肌肉瘤是儿童最常见的软组织肉瘤,滑膜肉瘤多见于青壮年,多形性高度恶性肉瘤、脂肪肉瘤和平滑肌肉瘤主要见于老年患者。
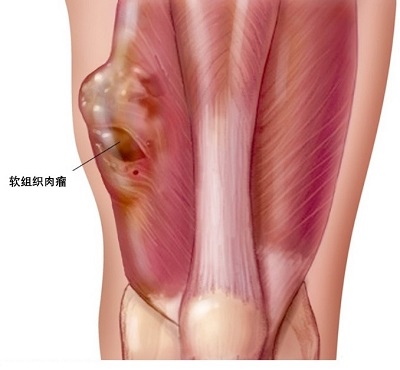
软组织肉瘤治疗手段
软组织肉瘤发病率低但危害性极大,转移和复发的可能性很高,很大一部分软组织肉瘤患者明确诊断时已经是晚期,晚期软组织肉瘤化疗的有效率为25~30%,5年生存率低于10%。
目前软组织肉瘤的主要治疗方法是手术、放疗及化疗。 对于早期发现的可接受切除手术的软组织肉瘤患者,根治性手术切除癌灶联合化疗或放疗可以帮助患者获得较高的5年生存率。而对于已经丧失手术机会的晚期软组织肉瘤患者,化疗是主要延长患者生命的手段,除胃肠间质瘤外,晚期软组织肉瘤的一线化疗方案为异环磷酰胺(IFO)联合阿霉素(ADM)。化疗的细胞毒性反应是全身性的,很多患者不能耐受,如阿霉素的累积剂量增加了心肌病和其他相关疾病的患病风险,严重影响患者的生存质量。
分子靶向治疗作为一种新兴的个体化治疗方法, 为一线化疗耐药或不宜手术的患者提供了新的解决途经。血管内皮生长因子受体(VEGFR)、血小板衍生生长因子受体(PDGFR)、干细胞因子受体(c-Kit)等以直接或间接地阻断肿瘤相关的信号通路,进而抑制肿瘤细胞的增殖。抗血管生成酪氨酸激酶抑制剂(TKIs)已被证明可延长晚期软组织肉瘤患者的无进展生存期。目前软组织肉瘤常用的靶向药物小分子化合物,包括安罗替尼、阿帕替尼、帕唑帕尼等。
肿瘤免疫治疗在软组织肉瘤中的应用
近年来,肿瘤免疫治疗成为新兴的研究热点。 肿瘤免疫治疗主要分为免疫检查点治疗和细胞免疫治疗两部分组成。免疫检查点治疗是解除肿瘤对免疫的耐受/屏蔽作用,让免疫细胞重新认识肿瘤细胞,对肿瘤产生攻击,例如PD-1抗体、PD-L1抗体、CTLA-4抗体等,有研究显示 PD-1抗体对多形性未分化肉瘤、脂肪肉瘤有着较好的疗效,但对平滑肌肉瘤、滑膜肉瘤或尤文肉瘤的疗效较差。细胞免疫治疗是把肿瘤的特征“告诉”免疫细胞,让它们去定位,并造成杀伤,例如CAR-T、TCR-T等。
CAR是嵌合抗原受体T细胞技术(CAR-T)的核心部件,赋予T细胞识别肿瘤抗原的能力,CAR的基础设计中包括一个肿瘤相关抗原结合区(通常来源于单克隆抗体抗原结合区域的scFV段),一个胞外铰链区,一个跨膜区和一个胞内信号区。
T细胞受体(TCR)嵌合型T细胞技术(TCR-T)转入的是T细胞受体,来自人体T细胞上分离得到的固有分子,包含两条肽链,均为跨膜蛋白,由二硫键相连。每条肽链胞外区各含1个可变(V)区和1个恒定(C)区,V区是TCR识别pMHC的功能区。胞质区很短,不具备转导活化信号的功能。跨膜区通过盐桥与CD3分子的跨膜区连接形成TCR-CD3复合体,转导活化信号至T细胞内。
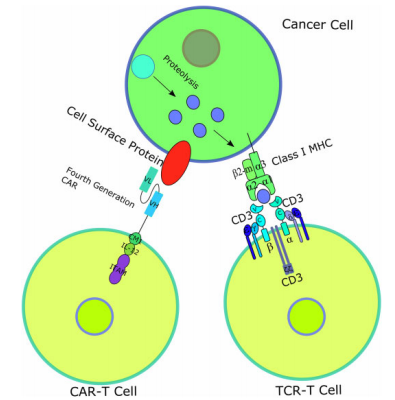
CAR-T和TCR-T结构示意图
打一个简单的比喻,CAR-T是一种“换头”技术,它把TCR的“头”直接换成一个特异性的抗体,这样T细胞就在抗体的指引下直接进攻癌细胞; T细胞受体TCR可以说只是简单地“理了理发”,通过部分基因修改的方法提高TCR对相应癌细胞相关抗原(Tumor Associated Antigen, TAA)的“亲和力”,从而对癌细胞的有利攻击。
目前CAR-T在血液肿瘤方面取得了积极效果,但在实体瘤治疗方面进展缓慢。与CAR-T相比,TCR-T却可以靶向全部抗原,包括胞外抗原(15%)、胞膜抗原(10%) 和胞内抗原(比如细胞质和核) ( 75%),目前发现的肿瘤特异性抗原 ( tumors pecific antigen,TSA) 即只在肿瘤细胞表达的抗原几乎全是胞内抗原,这使其在治疗过程中,可以通过选择特异性好的靶点和亲和力适中的受体的方法提高T细胞对肿瘤细胞的特异性识别能力,增加免疫细胞的应答、捕捉免疫逃逸,并降低T细胞对正常细胞的非特异性杀伤,让治疗更加精准。因此TCR-T在治疗实体瘤方面上的优势远远大于CAR-T。
Endo等报道指出在软组织肉瘤中,粘液样脂肪肉瘤显示出最高的NY-ESO-1阳性率(88%),其次是滑膜肉瘤(49%)。 另一项研究发现NY-ESO-1抗原表达于大约80%的滑膜肉瘤患者中。而在正常组织中NY-ESO-1不会被T细胞识别与杀伤,因此,NY-ESO-1 被认为是理想的肿瘤免疫治疗的靶点抗原。
在国内香雪精准医疗研发的TCR-T药物被命名为TAEST( TCR Affinity Enhanced Specific-T-cell Therapy), TAEST16001注射液获得国内首个TCR-T临床试验许可,适应症:用于治疗组织基因型为HLA-A*02:01,肿瘤抗原NY-ESO-1表达为阳性的软组织肉瘤。临床PI研究表明,TAEST16001治疗的病人其回输的T细胞在体内能够长时间维持,并体现较好的治疗效果。
在国际上Adaptimmune公司公布SPEAR T细胞(ADP-A2M4(MAGE-A4))试点研究中,5例滑膜肉瘤患者4例观察到部分反映,且几乎所有评估的滑膜肉瘤患者能够观察到肿瘤缩小。
综上所述,软组织肉瘤组织学分型多,发病率低,但危害大,目前手术是治疗STS最主要的手段,ADM + IFO 的一线化疗地位不可动摇,随着技术和医学的不断发展,新药物不断涌现,多种方法联合治疗,以及肿瘤免疫治疗的兴起,为患者提供了更多的治疗选择。
参考文献:
【1】崔抗, 赵瑞华,冯涵.软组织肉瘤靶向治疗药物的研究进展. 中国临床新医学 2019年4月第12卷第4期.
【2】王臻.晚期软组织肉瘤的治疗:机遇与挑战.Chinese Journal of Bone and Joint, January 2019, Vol 8, No.1.
【3】区裕升,郑红俊,钟时,李懿. TAEST16001: TCR亲和力增强型特异性T细胞免疫治疗. China Biotechnology,2019,39( 2) : 49-61.
【4】takuya kakimoto, akihiko matsumine, shinichi kageyama,kunihiro asanuma, takao matsubara,tomoki nakamura,takahiro iino,hiroaki ikeda,hiroshi shiku,akihiro sudo. Immunohistochemical expression and clinicopathological assessment of the cancer testis antigens NY‑ESO‑1 and MAGE‑A4 in high‑grade soft‑tissue sarcoma. ONCOLOGY LETTERS 17: 3937-3943, 2019
【5】Jianxiang Zhang ,Lingyu Wang. The Emerging World of TCR-T Cell Trials Against Cancer: A Systematic Review. Technology in Cancer Research & Treatment atment Volume 18: 1-13
文中图片源于参考文献和网络