资讯中心
作者:香雪生命科学研究中心-叶韵
发布时间:2021-08-28
阅读:17153
一、什么是GMP?
GMP是良好生产规范(Good Manufacturing Practice)的英文缩写。全称是Good Manufacturing Practice and Quality Control for Drug(药品)。当然广义的GMP还for Food(食品)、for Cosmetic(化妆品)。GMP是指在药品生产过程中实施质量管理,保证产品优质的一套完整的、系统的、科学的管理规范,是药品生产和质量管理的基本准则。
二、GMP的发展历史
GMP的提出和发展史,是一部人类制药用药和食品安全的血泪史。
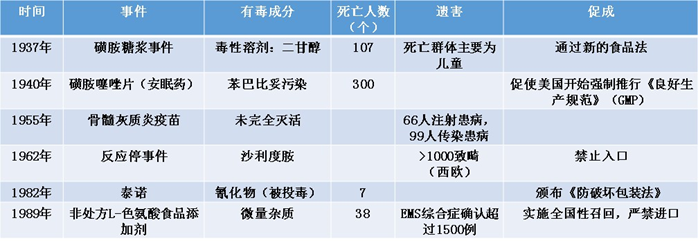
图一 药品安全危害事件
GMP的诞生不得不提到FDA(Food and Drug Administration)。自1848年美国联邦政府通过了药品进口法,要求美国海关总署检查并阻止劣质药物从海外进口,到1906年罗斯福总统签署《食品药品法》,人们终于意识到药品是可以假冒、掺假,食品在不卫生的环境下生产,即便加入防腐剂也是无效甚至有害的,而这些都需要从法律的途径去规范。
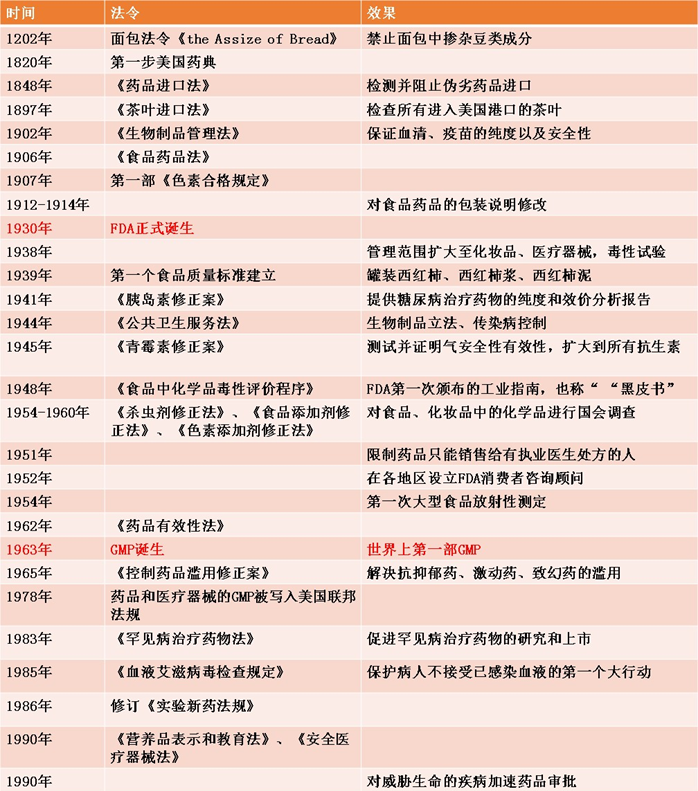
图二 美国FDA发展史
美国国会于1963年颁布了世界上第一部GMP, 1973年日本制药工业协会提出了自己的GMP,1974年日本政府颁布GMP,进行指导推行。1975年11月 WHO正式公布 GMP。 1980年日本决定正式实施GMP。
此后,英国、日本及大多数欧洲国家开始宣传、认识、起草本国的GMP,欧洲共同体委员会颁布了欧共体的 GMP。到1980年有63个国家颁布了GMP. 目前,已有100多个国家实行了GMP制度。 1998年国家药品监督管理局成立后,建立了国家药品监督管理局药品认证管理中心,并于1999年6月18日颁发了《药品生产质量管理规范(1998年修订)》。截止2000年年底,我国已有713家药品生产企业(车间)通过GMP认证。
我国主要的监管机构是CFDA(China Food and Drug Administration),是把食品安全办的职责、食品药品监管局的职责、质检总局的生产环节食品安全监督管理职责、工商总局的流通环节食品安全监督管理职责整合组建而成,负责药品、医疗器械、化妆品和消费环节食品安全的监督管理。2013年3月22日,食品药品监督管理局改成国家食品药品监督管理总局,英文简称由“SFDA”变成“CFDA”,简称 “中国食药监”。
三、GMP的目标
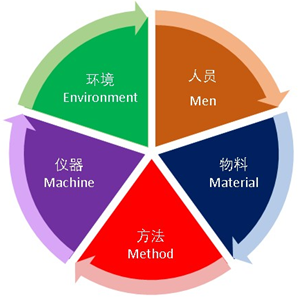
图三 GMP 5大要素
实施GMP的主要目标是通过控制药品生产过程中的5大要素,把人为的差错控制在最低限度,以保证产品的一致性、有效性以及安全性:
(1) 在管理方面
质量管理部门的建立;相互监督检查制度的建立;制订规范相应的SOP;整理和保管好记录;人员的配备、培训和管理。
(2) 在设备方面
合理的空间布局,不同品种操作必须有相应的时空分离。
2. 保证产品的安全性
(1) 在管理方面
定期操清扫作室和清洁设备;对生产人员进行严格的卫生教育;操作人员定期进行身体检查;限制非生产人员进入工作间等。
(2) 在设备方面
相应的机械设备(空调净化系统等)以及定期维护;操作室专用化;对直接接触药品的机械设备、工具、容器,选用对药物不发生变化的材质;对无菌操作区要进行微粒检查和浮游菌、沉降菌的检查,定期灭菌等。
3.保证高质量产品的质量管理体系
(1) 在管理方面
定期维修校正设备;检查生产工序各阶段的质量、有计划的合理的质量控制、质量管理实施计划、试验方案、技术改造、质量攻关要适应生产计划要求、追踪药品批号,并作好记录;在适当条件下保存出厂后的产品质量检查留下的样品、收集消费者对药品投诉的情报信息,随时完善生产管理和质量管理等。
(2)在装备方面
合理配备操作室和机械设备,采用先进的设备及合理的工艺布局;为保证质量管理的实施,配备必要的实验、检验设备和工具等。(2)
四、我们的产品

2018年12月29日,我司具有自主知识产权的高亲和性 T 细胞受体(TCR)的抗肿瘤TCR-T 细胞治疗新药----TAEST16001注射液产品获得国家药品监督管理局药品审评中心(CDE,Center for Drug Evaluation)药品临床试验申报(IND, Investigational New Drug Application)申请受理。
参考文献: